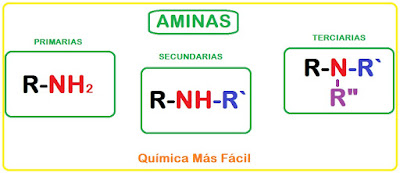
Las aminas pueden ser primarias, secundarias o terciarias, esto es según el número de enlaces a cadenas de carbono que tengan. El nitrógeno puede formar tres enlaces simples, formará enlaces con cadenas de carbono y el resto con hidrógeno.
Aminas primarias:
Se puede elegir entre dos formas para nombrarlas
1. Considerar el grupo R como un alcano con la terminación -amina y colocar a la amina el localizador más bajo posible.
2.Considerar como principal el grupo -NH2 y nombrar al grupo R como radical, la terminación también será -amina.
Ejemplo:
CH3-CH(-NH2)-CH3
1. Propanamina
2. Isopropilamina
Aminas secundarias y terciarias:
1. Para nombrarlas se toma como estructura principal aquella que contenga al radical R con mayor prioridad y para los otros radicales se usa la letra N- seguido del nombre del radical.
2. También se pueden nombrar usando los nombres de todos los radicales seguido de -amina.
Ejemplo:
CH3-CH2-CH2-CH2-NH-CH3
1. N-metilbutanamina
2. Butilmetilamina
Grupo secundario:
Cuando una amina actúa como grupo secundario se usa el prefijo amino-.
Ejemplo:
NH2-CH2-CH2-OH
2-Aminoetanol